CRISPR/Cas9技术科普篇
- 2025-02-21
- 26
2020年10月7日,瑞典皇家科学院决定将2020年诺贝尔化学奖授予德国马克斯·普朗克病原学研究所的Emmanuelle Charpentier博士以及美国加州大学伯克利分校的Jennifer A. Doudna博士,以表彰她们在基因组编辑领域的贡献。她们“研发了一种基因编辑方法”,重写了“生命密码”。这种技术工具名为CRISPR-CAS9。CRISPR-CAS9基因编辑技术一直是研究的关键和热点,通过该技术构建了很强的RNA引导的DNA靶向平台,其在基因组编辑、转录扰乱、表观遗传调控等各个领域广泛都有应用。
CRISPR/Cas技术简介:
Clustered regularly interspaced short palindromic repeats(CRISPR)——规律成簇的间隔短回文重复和CRISPR-associated protein 9(Cas9),共同组成了一套系统,即CRISPR/Cas系统,它是一种生物学工具,能以前所未有的精度来编辑基因组,就像文本编辑工具一样,能够通过“剪切和粘贴”脱氧核糖核酸(DNA)序列的机制来编辑基因组。
CRISPR/Cas9是细菌和古菌在长期演化过程中形成的一种免疫系统,用来抵抗外源遗传物质的入侵,为它们提供获得性免疫。CRISPR/Cas系统可以识别出外源DNA,并将它们切断,沉默外源基因的表达。正是由于这种精确的靶向功能,CRISPR/Cas系统已被开发成一种高效的基因组编辑工具。
在自然界中,CRISPR/Cas系统拥有多种类别,而CRISPR/Cas9系统是其中研究最深入,应用最成熟的一种类别。凭借着成本低廉,操作方便,效率高等优点,CRISPR/Cas9迅速风靡全球的实验室,成为了生物科研的有力帮手和基因编辑的强大工具。
CRISPR/Cas技术原理:
CRISPR序列由众多短而保守的重复序列区(repeats)和间隔区(spacer)组成。重复序列区含有回文序列,可以形成发卡结构。而间隔区比较特殊,它们是被细菌俘获的外源DNA序列。这就相当于细菌免疫系统的“黑名单”,当这些外源遗传物质再次入侵时,CRISPR/Cas系统就会予以精确打击。而在上游的前导区(leader)被认为是CRISPR序列的启动子。另外,在上游还有一个多态性的家族基因,该基因编码的蛋白均可与CRISPR序列区域共同发生作用。因此,该基因被命名为CRISPR关联基因(CRISPR associated,Cas)。Cas基因与CRISPR序列共同进化,形成了在细菌中高度保守的CRISPR/Cas系统。
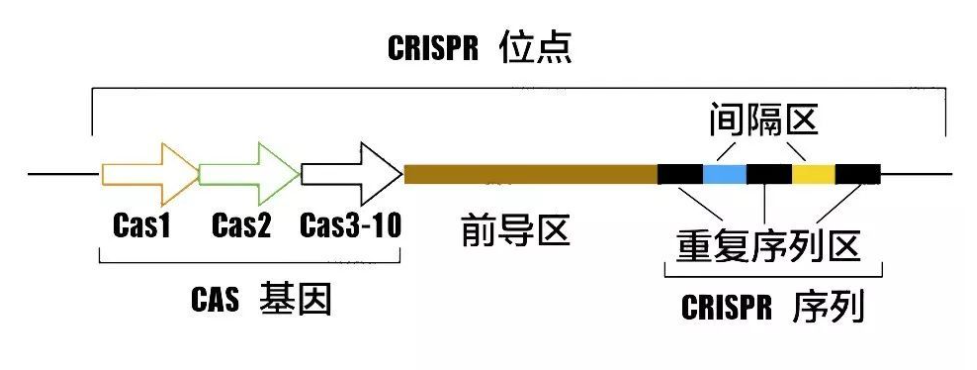
图1 CRISPR示意图
CRISPR/Cas技术应用:
CRISPR/Cas9基因组编辑技术为在几乎所有生物体中的大量应用操作打开了大门。自2012年这一编辑技术由沙尔庞捷和杜德纳开发以来,CRISPR/Cas9已用于寻找针对多种疾病(包括癌症和艾滋病等)的新疗法,以及培育植物新品种等。较之于siRNA文库和shRNA文库的knockdown, CRISPR-Cas9文库通过靶向基因的敲除konck out制造表型变化, 可以使用更加严苛的筛选标准, 更有效地去除假阳性; 而且有着成本低廉、构建简单、操作方便等优点。
根据CRISPR/Cas9精准攻击外源DNA的工作原理,可以实现基因敲除。如果在此基础上为细胞引入一个修复的模板质粒(供体DNA分子),就可以实现基因的定点突变。
对受精卵细胞进行基因编辑,并将其导入代孕母体中,可以实现基因编辑动物模型的构建,进而用于基因激活或失活,疾病模型构建,甚至是基因治疗。
此外,CRISPR-Cas9重要的应用之一是治疗遗传疾病。2014年,美国科学家Long等利用CRISPR-Cas9技术治愈了小鼠的杜氏肌营养不良症。安全高效的CRISPR-Cas9技术让我们看到了人类遗传疾病的治疗的新方向。
卡梅德生物依托先进的技术和经验丰富的科研团队,可为客户提供系统的CRISPR/Cas9敲除细胞系构建服务。我们与国内知名研发单位合作推出完备的CRISPR/Cas9载体系统,包括单敲除、双敲除、缺口酶、慢病毒敲除载体和敲除载体库等体系,并且每一个载体系统都有不同的标签(EGFP/RFP/Puro/Neo)可供选择,能够为客户提供快速、准确的基因敲除项目服务。
- CRISPR/Cas9
- 基因编辑
- 表观遗传调控
- 目的基因敲除细胞系的构建
-
 400-621-6806
400-621-6806 -
 614353794
614353794 -
 周一至周五 9:00-18:00
周一至周五 9:00-18:00 -

-
 0
0
-





